“
背景简述
mRNA 疫苗,是一种核酸疫苗。由于利用的是病毒基因序列而非病毒本身,因此 mRNA 疫苗不带有病毒成分、没有感染风险、针对病原体变异反应速度快,是继灭活疫苗、减毒活疫苗、亚单位疫苗和病毒载体疫苗后的第三代疫苗。
mRNA 能够有效激起体液免疫和细胞免疫反应的特性使其在传染病预防、肿瘤治疗、蛋白补充和基因治疗等领域得到充分的应用,在生物医药行业拥有巨大的市场潜力。新冠肺炎来袭,促使 mRNA 疫苗开发技术在传染病领域飞速发展。
疫情爆发不到一年,辉瑞/BioNTech和Moderna 便快速发布了高效的 mRNA 疫苗,并获得紧急使用授权, 而该疫苗也在临床试验和现实应用中展现出了高强的保护效力。Nature 子刊最新数据显示,目前全球大约有 90 个 mRNA 疫苗研发机构,137 种 mRNA 候选疫苗正在研发中,76% 处于临床前,24% 处于临床试验中。
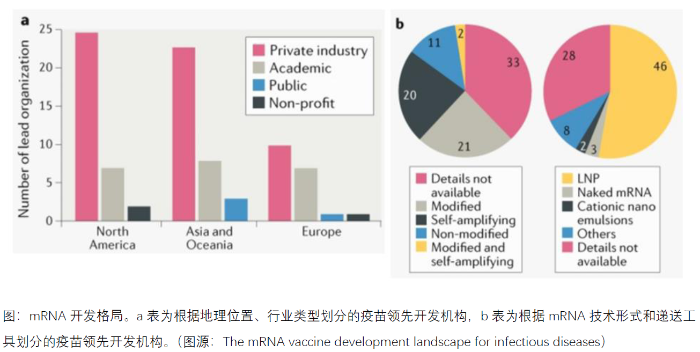
截至目前,国内沃森、斯微、复星、辉瑞、中国人民解放军军事医学科学院均有申报新型冠状病毒肺炎 mRNA 疫苗产品。
控制传染病流行的有力武器
为预防性疫苗开发提供新思路
与传统疫苗相比,核酸疫苗在传染病防治领域有以下几点优势:
1
生产周期短:
核酸疫苗拥有较短的开发时间,且生产工艺简单,易于批量生产。在针对大型传染病防控工作中能够迅速铺开应用,如埃博拉、新冠肺炎、流感等。
2
快速反应能力:
核酸疫苗开发具有较强灵活性,可基于成熟的技术平台制造变体疫苗或多价疫苗,扩大保护范围。面对病毒变异,仅需更换抗原序列,4-6 周便可实现更新,能够快速投入一线。
3
安全性更好:
相较基于 DNA 的疫苗工艺,mRNA 无需进入细胞核,因此可以降低外源性感染或插入突变的潜在风险。此外,mRNA 半衰期和固有免疫原性可通过修饰、递送调节,进一步提高 mRNA 疫苗安全性。
4
给预防性疫苗开发提供新思路:
目前市场上的传统疫苗无法应对 RSV、HIV-1、单纯疱疹病毒等引发慢性或反复性感染的传染性疾病,核酸疫苗是新的研究方向。针对已有 mRNA 产品如狂犬疫苗等,随着技术革新,产品性能也将得到进一步优化升级。
mRNA 疫苗生产力需快速提高
目前制约因素或将进一步取得突破
新冠疫情爆发前,核酸疫苗的开发主要集中在高成本的个性化癌症疫苗方面。而面对新冠疫情的冲击,为满足数十亿剂的生产技术需求,需要快速扩大 mRNA 疫苗生产能力,以下制约因素或将进一步取得突破。
1
关键技术有待突破:
当前阻碍国内核酸疫苗产业化发展的技术因素包括 mRNA 递送载体技术、mRNA 的加帽加尾、序列优化及核酸修饰技术等。
2
疫苗储存条件要求较高:
已上市的两款 mRNA 疫苗都需要在极低温度下储存(辉瑞/ BioNTech 疫苗储存温度在 -80℃到 -60℃,Moderna 疫苗储存温度需要 -20℃),严苛的存储条件增加了疫苗在生产、运输、储存环节的成本,从而限制了 mRNA 疫苗大规模的应用。冻干作为一种替代储存的工艺正在研发中。
3
制造工艺需要改进:
国内核酸原料供应商已具备一定规模,部分公司酶原料得到国外 mRNA 疫苗开发商认可,作为原料供应商的同时拥有较大的成本优势。但在生产设备提供方面,由于国内产业化起步较晚,与国际该行业仍存在一定差距。
化信观点
传统疫苗的开发和审批速度缓慢,面对埃博拉和寨卡病毒等大规模疫情时,难以起到及时防治作用。经验表明搭建更快捷有效的疫苗开发平台至关重要。mRNA 疫苗凭借优越的开发速度和临床有效性在新冠肺炎大流行时脱颖而出,可以预见,未来 mRNA 疫苗平台可在预防和控制病毒大流行上迅速发挥积极作用。
COVID 疫苗产品改进优化取决于其安全性、耐受性和免疫原性方面的突破。Nature 显示辉瑞/BioNTech 和 Moderna mRNA 新冠疫苗均有使用 LNPs 配制的核苷修饰技术,帮助调控 mRNA 疫苗未来的病原体。
在疫情冲击下,国内 mRNA 疫苗技术急速发展。同时 mRNA 疫苗也能填补传统疫苗在部分传染病领域的空缺。目前国内行业上游核酸原料供应趋于成熟,下游设备供应跟国际相比仍有一定差距。此外,疫苗储存条件是限制 mRNA 疫苗大批量应用的阻碍,国内疫苗开发关键技术亟待突破。
尽管目前 mRNA 技术平台仍面临许多挑战,但不可否认,未来该技术在应对突发传染病爆发时将拥有巨大潜力。












