“
背景简述
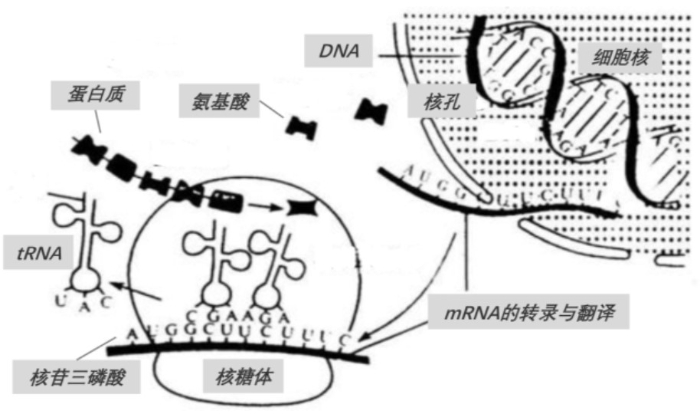
mRNA 又称为信使 RNA,是由 DNA 的一条链为模板转录而来,携带遗传信息,能指导蛋白质合成的一类单链核糖核酸。理论上,mRNA 拥有能够合成任意一种蛋白质的潜力,由于其具有经济、安全、快速、灵活等特点,mRNA 药物在传染病预防、癌症和包括罕见病在内的多种疾病治疗领域具有巨大的应用潜力。
近几年,通过在 mRNA 序列中引入经过修饰的核苷,并开发出 RNA 递送系统,解决了 mRNA 发现之初,不稳定性和免疫原性等问题。
将 mRNA 制成疫苗或者药物,相当于送出一张可以在人体内生成药物工厂的“施工图纸”,根据这张图纸,mRNA 可以在细胞内翻译表达而无需进入细胞核,因此相比于 DNA 药物,mRNA 药物并没有整合人体 DNA 的风险,也可作用于传统蛋白药物(如抗体等)无法触及的胞内靶点。因此从制药行业的角度来看,mRNA 是一种非常有潜力的候选药物,可以满足基因治疗、癌症治疗以及开发疫苗等的需求。
常见的 mRNA 递送系统
由于 mRNA 本身带有大量的负电荷,是较强的极性分子,不能自行穿过细胞膜。因此 mRNA 如何递送是一个需要解决的难题。将 mRNA 包裹起来,打包送到细胞内,是人们首先想到的办法。纳米脂质体(LNP,Lipid nanoparticles)、多肽纳米粒子和半乳糖胺配体(GalNac)等作为常用的包埋物,与 mRNA 形成纳米尺度的颗粒状多聚体很容易就进入到细胞内。其中,LNP 最开始时是为基因治疗而开发的递送 DNA 的物质,含有可离子化的脂质体、聚乙二醇和胆固醇等,后期才应用到 mRNA 的递送中。
比较成熟的 LNP 系统 有 Arbutus 的 DLin-MC3-DMA 和 Alnylam 公司的 DLin-DMA等,前者以 5000 万美元转让专利给了 Moderna 公司。相对其他类型的核酸药物递送系统而言,LNP 具有很多优势,比如核酸包封率高并且能够有效转染细胞,组织穿透性强,细胞毒性和免疫原性低,更有利于递送药物等优势,这些优势使 LNP 成为出色的核酸递送系统。
美国 Alnylam 公司是最早采用 ESC-GalNac 递送技术 的企业,这是一种靶向修饰技术,其产品 Lumasiran 作为一种皮下注射的治疗原发性 1 型高草酸尿症(PH1)的 RNAi 药物,已在欧洲获批上市。国内瑞博生物有自主研发的 GalNac 递送技术平台,该平台基于 GalNAc 与小核酸共价连接,GalNac 可以与实质肝细胞表面的去唾液酸糖蛋白受体(ASGPR)特异性结合,实现细胞的快速胞吞。该技术具有高度的肝靶向特异性,给药后高效富集到肝组织,进入其他组织的量非常少。
外泌体(Exosome)小核酸递送领域,CODIAK 公司研发的外泌体载 siRNA 和反义核酸药物目前已有进入二期临床的品种。EVOX 公司获得武田制药和礼来制药的大量投资。外泌体可有效解决跨膜和内涵体逃逸问题是未来核酸药物递送的最具开发潜质的载体。
AVV 载体 具有良好的安全性和较高的递送效率,在使用 AVV 载体的基因药物中,已获批上市分别是 Glybera,Luxturna 和 Zolgensma。
预防性疫苗开发进度较快
治疗性疫苗存在利基市场空间
Nature Reviews Drug Discover 发表的一篇关于 mRNA 药物市场分析的文章,对 31 家公司的 mRNA 管线进行了梳理。 76 款预防性疫苗中,22 款用于预防 COVID-19 感染;32 款治疗性疫苗中,21 款与癌症有关。
从产品开发进度上看,预防性疫苗 已经有产品上市或者授权紧急使用,分别来自辉瑞/BioNtech 和 Moderna,其他大多数产品处于临床一期或者临床前开发阶段。治疗性疫苗 目前仍是 mRNA 药物中的小众产品,但基于患者群体规模以及其在靶向多种肿瘤相关抗原治疗模式中占据主导地位的可能性,未来或拥有较大商业潜力,是 mRNA 产品的一个利基市场空间,但需要充分考虑临床开发、监管和制备的风险。当下,mRNA 治疗性疫苗主要集中在免疫肿瘤学 (IO) 上,越来越多的公司开始关注与 IO 药物(如 PD1/PDL1 阻滞剂)的联合策略,用于疾病负担较低且免疫系统仍然有效患者的早期治疗。
受新冠疫情影响,目前 mRNA 在研管线主要集中在预防性疫苗,77% 的 mRNA 公司至少有一种预防性疫苗在研发中。
治疗性药物或将是 mRNA 产品的机会性领域。涉及多种适应症,长期机会将取决于递送系统和基因编辑等领域的技术进步,可喜的是研究人员已经为此开发出脂质纳米粒等基于创新材料的递送解决方案。
国内多家企业布局 mRNA 药物
mRNA 巨大的增量市场吸引了大量药企争相布局。就国内而言,传统巨头布局 mRNA 疫苗的包括国药,恒瑞,石药,百济神州;通过与国外公司合作进行 mRNA 研发的企业包括复星医药(德国疫苗公司 BioNTech 授权),南京奥罗生物科技有限公司(与比利时 eTheRNA 合作),云顶新耀(与加拿大疫苗开发商 Providence Therapeutics 达成全面协议)。
具有独立研发能力的初创核酸药企 包括斯微,艾博,丽凡达,蓝鹊,启辰生物,新合生物,本导基因等。斯微,艾博(与云南沃森,军事医学院合作),丽凡达,复星,是国内仅有的获得新冠 mRNA 疫苗临床批件的企业。其中,云南沃森的新冠 mRNA 疫苗在进行 III 期临床试验,复星新冠 mRNA 疫苗在进行 II 期临床试验,斯微和丽凡达的新冠 mRNA 疫苗处于I期临床试验。
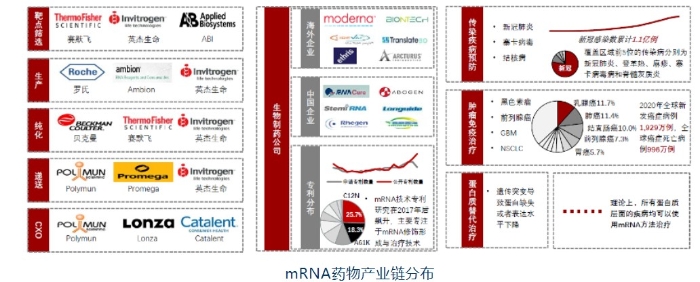
mRNA 药物产业链分布
化信观点
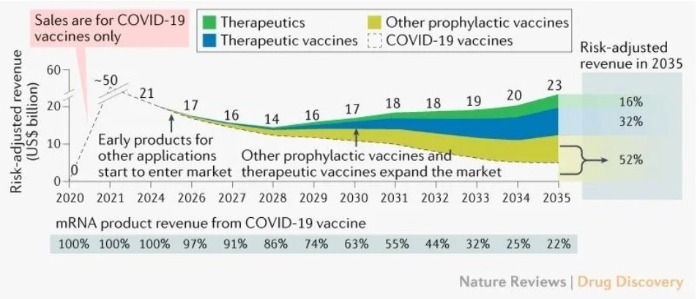
mRNA 市场潜力巨大,以新冠疫情为契机,目前尚处于起步阶段。2021 年预计的市场规模为 50 亿美元,但均来自于新冠疫苗。根据 Nature Reviews Drug Discovery 预测,2035 年风险调整后,预计 mRNA 市场规模会攀升到 230 亿美元。其中,新冠疫苗比例将下降至 22%,治疗性疫苗比例将达 32%,其他感染性疾病 mRNA 疫苗比例占 30%,治疗性 mRNA 药物比例约为 16%。肿瘤、呼吸系统疾病(主要是囊性纤维化)和罕见疾病的全球管线资产平均销售额峰值分别约为 11 亿美元、18 亿美元和 5 亿美元。
随着新冠疫情逐渐缓解以及默沙东、辉瑞新冠口服药的一跃而出,新冠 mRNA 疫苗赛道已没有多少市场留给其他药企,许多初创核酸药企需要开拓其他市场方向,例如其他传染病疫苗和肿瘤治疗,基因编辑等领域。风口过后,真正能够存活发展的企业,必然要具备独立的研发能力,强大特异性的递送系统和稳定高效的表达设计,缺一不可。